-
Об ассоциации
- Руководство ассоциации
- Региональные отделения
- Присоединиться к ассоциации
- Уставные документы
- Отзывы об ассоциации
- Контакты
- Взносы в ассоциацию
- Партнёры ассоциации
- Сотрудничество
- СМИ об ассоциации
- Аккредитация СМИ
- Отчётность
- Проекты
- Горячая линия
- Конкурс журналистских работ
- История моей победы
- Онкопатруль
- Группа взаимопомощи
- Проект «Силы есть»
- ОчУмелые ручки
- Жизнь после диагноза
- Танцетерапия
- #СпастиЖизнь
- Онконет
- Проект Важно услышать
- Пациентоориентированный цифровой онкоцентр
- Волонтерское движение
- Занятия по скандинавской ходьбе
- Пациентам
-
О раке
- Рак и его типы
-
Лечение
- Химиотерапия
- Лучевая терапия
- Хирургическое лечение
-
Клинические исследования
- Новые методы лечения рака
- Набор в клинические исследования
- Что такое клинические исследования и для чего они проводятся?
- Кто может принять участие в клиническом исследовании?
- Как проводятся клинические исследования?
- Что такое информированное согласие?
- Для чего используется плацебо при проведении клинических исследований?
- Где проводятся клинические исследования и как я могу получить информацию об исследованиях, в которых я могу принять участие?
- Гормонотерапия (эндокринотерапия)
- Поддерживающая терапия
- Осложнения лечения и их коррекция
- Лечебное питание
- ВАХД-инновационный метод лечения
- РНЦХ имени акад. Б.В. Петровского
- Радионуклидная альфа-терапия
- Профилактика нежелательных явлений
- Это надо знать
- Помощь
- Профилактика
- Полезная литература
- ОМС
- Медико-социальная экспертиза
- Сессии на конференциях
- Опросы
- Адреса
- Вопрос ответ
- Уход за кожей онкопациента
Онконет
Проект ОНКОНЕТ реализуется с использованием гранта Президента Российской Федерации на развитие гражданского общества, предоставленного Фондом президентских грантов.

Использование цифрового сервиса ОНКОНЕТ для дистанционного мониторинга онкологических пациентов на иммунной и таргетной терапии в условиях пандемии.
Каприн А.Д. – Доктор медицинских наук, профессор, академик Российской академии Генеральный директор ФГБУ «НМИЦ радиологии» Минздрава России, директор МНИОИ имени П.А. Герцена, главный внештатный онколог Минздрава России
Шинкарев С.А. – д.м.н., профессор, главный врач Липецкого областного онкологического диспансера ГБУЗ ЛООД (научный руководитель проекта ОНКОНЕТ)
Орлова Р.В - д.м.н., руководитель 11-ого химиотерапевтического отделения Городского клинического онкологического диспансера Спб , заведующая кафедрой онкологии Санкт-петербургского государственного университета.
Каргальская И.Г. – руководитель Комитета "Пациентоориентированная телемедицина" при Всероссийском Союзе пациентов (технический директор ОНКОНЕТ)
Зингерман Б.В. – научный руководитель ООО "Телепат", программный директор Онконет
Боровова И.В – Президент Ассоциации онкологических пациентов «Здравствуй»
Шинкарева Е.В. – заведующая 1 отделением химиотерапии ГБУЗ ЛООД
Нозик А.В. – ведущий разработчик ОНКОНЕТ
ВведениеОнкологические пациенты страдают от множества симптомов, вызванных как самим заболеванием, так и побочными эффектами противоопухолевого лечения. Многие симптомы остаются незамеченными по причине удаленного местожительства пациента, значительных перерывов между визитами к врачу, различий в индивидуальном анамнезе заболевания и недостаточной коммуникации между врачом и пациентом [1-7]. В целом ухудшение симптомов указывает на прогрессирование рака или серьезные нежелательные явления и служит причиной снижения выживаемости [8].
Повсеместное рутинное использование разными категориями пациентов смартфонов и планшетов делает крайне актуальной идею оперативного сбора индивидуальных данных о состоянии здоровья пациента с использованием каналов мобильной связи [9].
С 2016 года в США и Европе начинают активно использовать цифровые инструменты, вовлекающие пациентов в сбор дополнительной информации о своем состоянии и передачу ее в электронном виде лечащему врачу, что позволяет своевременно и непрерывно собирать и анализировать в автоматическом режиме данные о самочувствии пациента, находящегося за пределами лечебного учреждения [10-16]. В случае если такой сбор актуальных симптомов еще и сопровождается возможностью автоматических экстренных уведомлений («алармов»), посылаемых в опасных ситуациях пациенту и его лечащему врачу, это дает пациенту шанс своевременно среагировать на проблему, связаться с врачом и снизить возможность развития ургентных состояний или вовремя вызвать Скорую помощь.
В настоящее время существуют убедительные доказательства эффективности такого мониторинга [17-20].
|
|
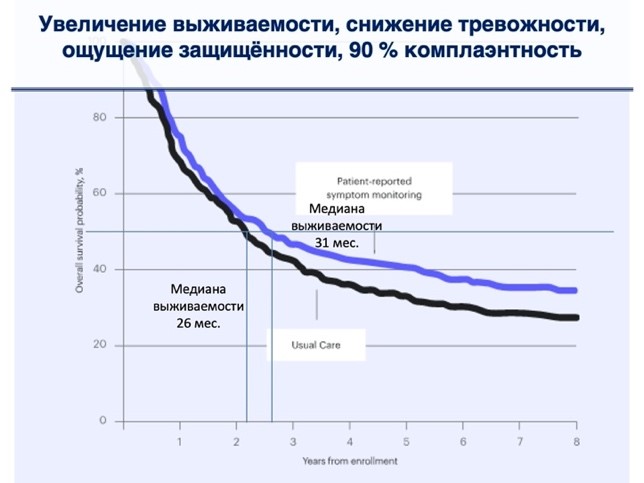
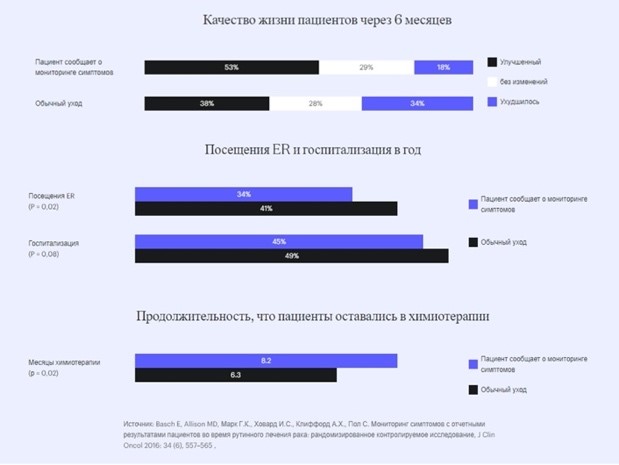
Так по данным рандомизированного клинического исследования [20], в котором принимали участие 766 пациентов с различными формами рака (в т.ч. пациенты старше 55 лет с минимальным уровнем компьютерной грамотности), информировавших врача онлайн о своих симптомах в процессе лекарственной терапии, зафиксировано более высокое качестве жизни пациентов, снижение посещений отделений неотложной помощи и увеличение медианы выживаемости на 5 месяцев в сравнении с теми, кто не пользовался этим инструментом. По словам Harold J. Burstein, MD, PhD, FASCO, ASCO ExpertDana-FarberCancerInstitute: «Если бы какой-нибудь препарат имел преимущество в выживании такого масштаба, он был бы в розничной продаже по цене в сотни тысяч долларов. Есть очень мало лекарств, которые дают такие преимущества выживания и улучшения качества жизни! При этом, как правило, мы пренебрегаем инвестированием в электронное общение с пациентом» [21].
Однако, инструменты такого электронного дистанционного мониторинга используются пока еще достаточно редко. К настоящему времени в России не проводилось масштабных работ и рандомизированных исследований по дистанционному мониторингу онкологических пациентов. Приведенное в данной статье исследование проводилось с начала 2019 годов в Липецком областном онкологическом диспансере. В статье приведены первые результаты этого исследования.
Исследование проводилось с использованием сервиса ОНКОНЕТ, разработанного ООО «ТелеПат» [22], и внедряемого в практику российского здравоохранения Ассоциацией онкологических пациентов «Здравствуй» [23] при поддержке Фонда Президентских грантов N19-1-022113.
Материалы и методы
Для дистанционного мониторинга пациентов на различных этапах онкологического лечения использовалась специализированная платформа ОНКОНЕТ (разработанная ООО «ТелеПат» [22]). Платформа использовалась в следующем порядке:
- Лечащий врач подключал своего пациента к системе дистанционного мониторинга, назначая ему набор специализированных опросников и периодичность (календарь) направления их пациенту.
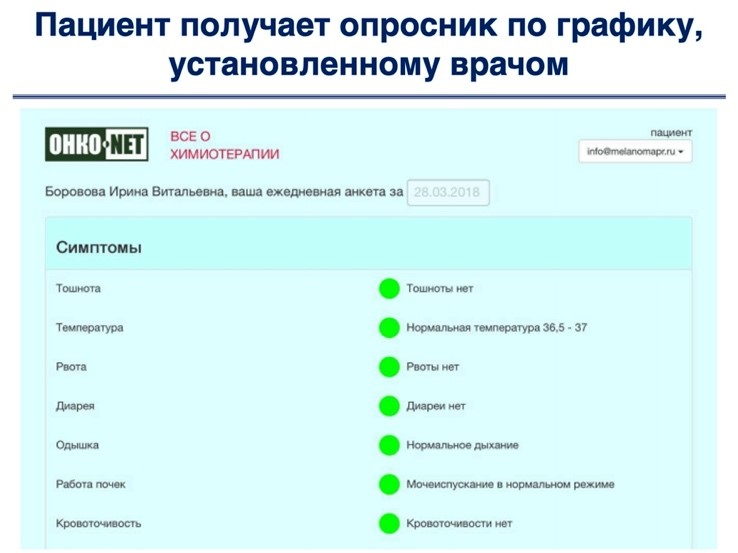
- Пациент получал по электронной почте ссылку на опросник в соответствии с графиком, установленным врачом, и отвечал на вопросы в нем (опросники адаптированы под мобильные телефоны и пациентоориентированы).
- Если пациент в процессе заполнения опросника указывал опасный или критический симптом, то он сразу же получал уведомление «Немедленно вызовите скорую помощь!» или «Срочно обратитесь к лечащему врачу!».
- По результатам заполнения всего опросника в желто-зеленом коридоре пациент также получал набор рекомендаций в виде ссылок на информационные материалы или видеошколы, размещенные на том же портале ОНКОНЕТ. Эти материалы содержали советы по уходу и организации образа жизни, позволяющие снизить влияние отмеченных пациентом некритичных симптомов.
- В системе ОНКОНЕТ также имеется возможность для пациента прикрепить дополнительные документы (например, анализ, выполненный в другой лаборатории) и написать врачу сообщение, описав симптом или проблему, не включенные в опросник.
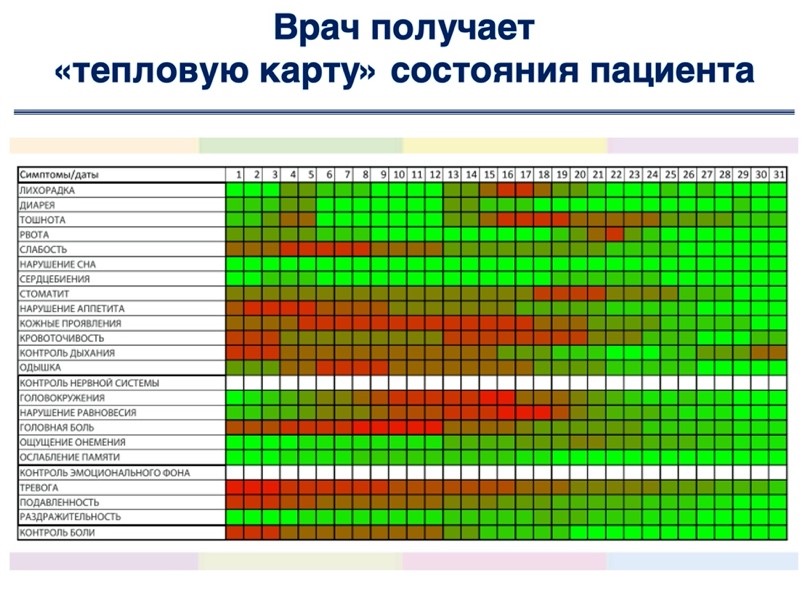
- Результаты заполненных опросников сохранялись на закрытом сервере и периодически направлялись врачу в виде специальной «тепловой карты», демонстрирующей динамику симптомов у пациента.
- Периодически (по установленному им графику) врач получал сводку по всем своим пациентам, состоящим на дистанционном мониторинге. Сводка ранжировалась по общей комплексной тяжести отмеченных пациентом симптомов, с тем чтобы врач мог более оперативно оценить состояние самых тяжелых пациентов и принять соответствующие меры. Алгоритм комплексной оценки был разработан авторами с учетом весовых коэффициентов различных симптомов, указанных врачами-онкологами.
- В случае необходимости врач прямо в системе ОНКОНЕТ мог написать пациенту дополнительную рекомендацию, пригласить на очный прием или переслать ссылку на дополнительный материал с рекомендациями. Все полезные врачу информационные материалы (в том числе и те, которые можно послать пациенту) объединены, в «Библиотеку врача», которая активно используется при работе с системой.
|
|
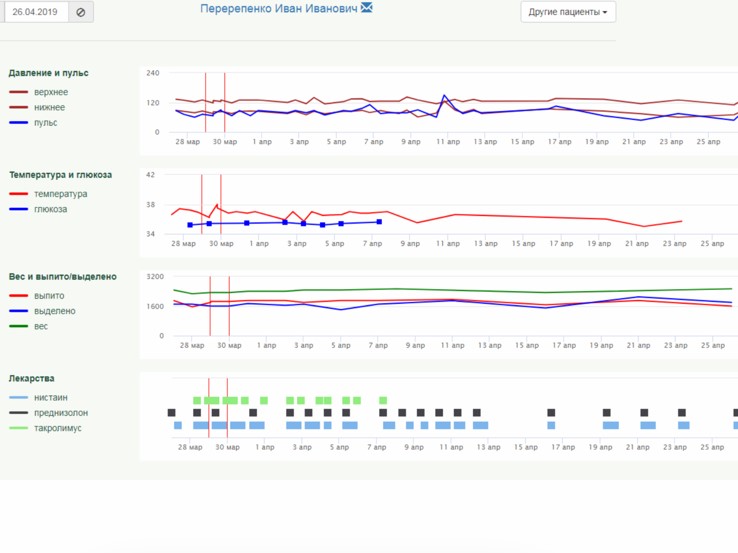
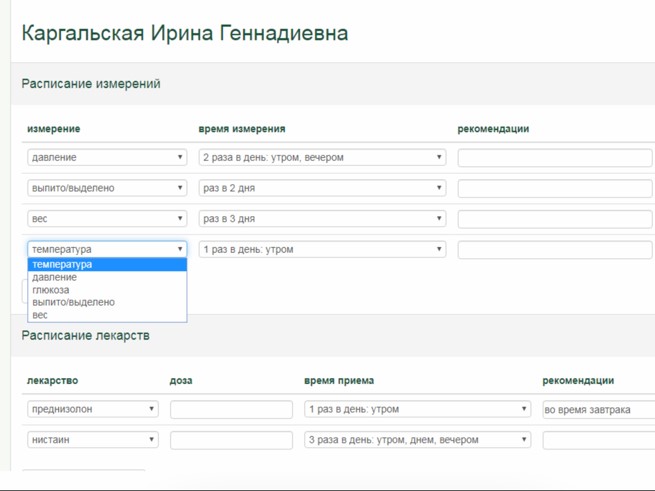
Дополнительно к опросникам врач может назначить пациенту один или несколько раз в день еще и контроль параметров (давление, температура, глюкоза, вес), а также напоминания о приеме лекарств с подтверждением приема. Измеренные пациентом показатели и отметки о приеме лекарств также включаются в «тепловую карту» в виде понятных динамических кривых
|
|
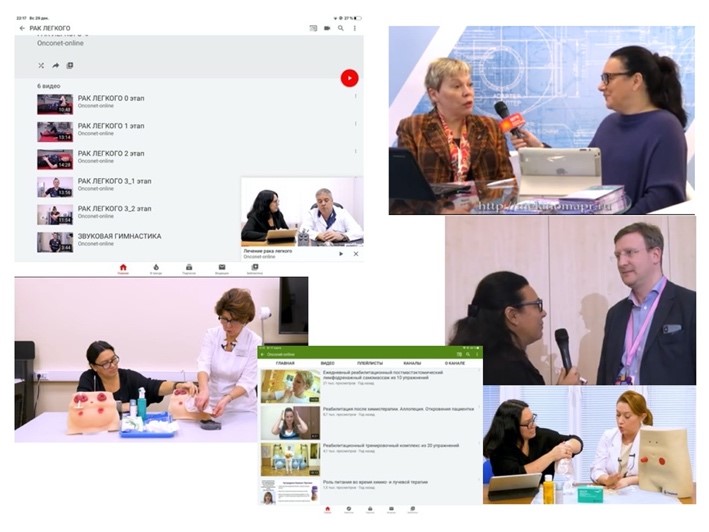
Также в ОНКОНЕТ интегрирована «Библиотека пациента», содержащая 1250 страниц пациентоориентированного информационного контента и телеподдерживающих пациентских школ от ведущих экспертов по особенностям и видам лечения, по нозологиям, правилам жизни и питания, реабилитации и уходу.
Основой описанной выше системы ОНКОНЕТ являются специализированные опросники, разработанные врачами-онкологами для дистанционной оценки состояния пациента.
Одной из главных проблем при составлении опросников было преобразование описаний оценок в понятный для пациента язык. Любые критерии, которые не может сообщить пациент,
были исключены из опросников. При разработке опросников для оценки их понятности привлекались представители пациентских сообществ. Понятность опросников тестировалась на больших группах пациентов.
|
|
В системе ОНКОНЕТ разработан специальный инструментарий, позволяющий оперативно добавлять новые и модернизировать существующие опросники. Это обеспечило создание достаточно большого количества профильных опросников, позволяющих контролировать важные симптомы и побочные явления, свойственные конкретным методам лечений и состояниям онкологического пациента.
На сегодняшний день в систему включены опросники и их группы, приведенные в Таблице 1. Опросники создавались в разное время и использовались с разной интенсивностью для разных групп пациентов, поэтому количество заполненных на сегодняшний день опросников каждого вида, указанное в таблице (на момент публикации), существенно рознится.
Важно отметить, что с началом пандемии COVID-19 и публикации Минздравом информации об особой уязвимости пациентов, проходящих химиотерапию, в систему был добавлен опросник по симптомам COVID-19. Специальной рассылкой врачи были уведомлены о возможности подключить его своим пациентам. Некоторые опросники на момент публикации были подготовлены, но еще не тестировались пациентами.
|
Вид опросника |
Количество включенных вопросов |
Заполнено пациентами (шт) |
|
Коронавирус |
||
|
Контроль симптомов COVID-19 |
11 |
186 |
|
Мониторинг пациентов на лекарственной терапии |
||
|
Базовый мониторинг пациентов на химиотерапии |
30 |
24 |
|
Мониторинг пациентов на иммунотерапии |
19 |
100 |
|
Мониторинг пациентов на таргетной терапии для MEK/BRAF |
15 |
|
|
Мониторинг пациентов на таргетной терапии (анти EGFR) |
13 |
|
|
Мониторинг пациентов на таргетной терапии (анти АЛК) |
17 |
54 |
|
Мониторинг на таргетной терапии (анти VEGF) |
|
|
|
Общие симптомы |
15 |
6285 |
|
Рак легкого |
||
|
Рак легкого – постоперационный мониторинг |
20 |
11 |
|
Мониторинг пациентов с раком легкого на химиотерапии |
33 |
12 |
|
Рак молочной железы |
||
|
Постоперационный мониторинг РМЖ |
14 |
20 |
|
Мониторинг пациентов с РМЖ в отсроченном периоде |
13 |
1116 |
|
Контроль позднего лимфатического отека при РМЖ |
4 |
471 |
|
Колоректальный рак |
||
|
Постоперационный мониторинг пациентов с колоректальными ЗНО |
26 |
28 |
|
Мониторинг третьей линии терапии пациентов с метастатическим колоректальным раком |
25 |
328 |
|
Дополнительные анкеты |
||
|
Мониторинговая постоперационная анкета |
19 |
139 |
|
Контроль нервной системы |
5 |
2926 |
|
Контроль эмоционального фона |
5 |
3873 |
|
Контроль недостаточности питания |
5 |
2287 |
|
Контроль количества съеденного |
6 |
2586 |
|
Контроль интенсивности боли для вербальных пациентов |
5 |
561 |
|
Контроль интенсивности боли для невербальных пациентов |
5 |
63 |
|
Контроль анемии |
1 |
845 |
|
Контроль психологического состояния |
||
|
Госпитальная шкала тревоги и депрессии (HADS) |
14 |
21 |
|
Шкала Бека на уровень депрессии |
21 |
|
|
Шкала Цунга |
20 |
|
|
Мониторинг хирургических осложнений в постгоспитальный период |
||
|
Рак прямой кишки |
26 |
|
|
Рак толстой (ободочной) кишки |
24 |
|
|
Опухоли ЖКТ |
21 |
|
|
Онкогинекология |
21 |
|
|
Онкоурология |
22 |
|
Сами опросники включали в себя указанное в таблице количество вопросов и варианты ответов в одной из 2-х форм:
- Варианты ответа в описательной форме, ранжированные от нормы (отмеченной зеленым), до критического состояния (отмеченного красным).
- В виде балльной оценки от 0 до 10 (выбираемой пациентом с помощью движка).
Пациент получал опросник, в котором все значения были предустановлены в значение «нормы» (зеленое). Но если пациент ощущал проблемы по какому-то из симптомов, то он мог открыть этот вопрос и указать значение, наиболее соответствующее его состоянию. Такой подход был избран для исключения «гипердиагностики» своего состояния пациентами.
По результатам проведенных опросов пациенты указывали:
- «нормальное» состояние симптома в 89.9 % случаев (разброс от 8% до 100% по разным симптомам);
- состояние с определенными отклонениями от «нормы» в 8% случаев (разброс от 0% до 92%);
- тяжелые и критические состояния в 2.1% случаев (разброс от 0% до 47%).
Система тестировалась в течение 2018-2020 годов в 22 медицинских организациях в 10 регионах России. В тестировании системы участвовали (на момент публикации) 174 врача и 382 пациента. При этом первоначально к системе было подключено 460 пациентов, 78 из которых – 17% – так и не начали отвечать на поступающие к ним опросники. Реально участвовавшие в мониторинге 382 пациента ответили на 92% поступивших к ним опросников, что свидетельствует о высоком уровне востребованности системы пациентами. Всего на момент публикации пациентами было заполнено 21936 опросников (в среднем – 57 на пациента) и сообщено о 193248 симптомах (более 500 в среднем на пациента).
Наибольшее число пациентов протестировано в Липецком областном онкологическом диспансере – 206 пациентов. Данные по этим пациентам более детально обработаны, сопоставлены с группой сравнения и приведены в следующем разделе.
Результаты
В течение 2018-2019 годов в Липецком областном онкологическом диспансере с помощью системы ОНКОНЕТ проводился в пилотном режиме дистанционный мониторинг онкологических пациентов. В проекте принял участие 61 врач, за весь период было зарегистрировано 415 пациентов . Был организован детальный дистанционный мониторинг 206 пациентов. В исследовании участвовали пациенты с раком молочной железы, раком легкого, шейки матки и яичников, предстательной железы, щитовидной железы, почки, желудка и колоректальным раком, лимфомы Ходжкина и неходжкинкой лимфомы.
Общие отзывы о работе системы, полученные как от врачей, так и от пациентов, были весьма положительными. Однако для объективной оценки результатов решено было провести сравнение медицинских результатов с контрольной группой пациентов, находящейся на обычном наблюдении у районного онколога и не использовавшей дистанционный мониторинг состояния лечащим врачом. Поскольку исследование изначально не планировалось как рандомизированное, для сравнения была ретроспективно подобрана группа пациентов (206 человек в группе Онконет и 209 человек в контрольной группе ), сходная по составу диагнозов и стадий заболеваний, используемым схемам лечения, а также по половозрастному составу. В этих группах оценивалась частота осложнений и побочных реакций в процессе лечения, а также важнейший показатель – перенос или отсрочка очередного курса химиотерапии.
Результаты сравнения групп приведены на Диаграмме 1.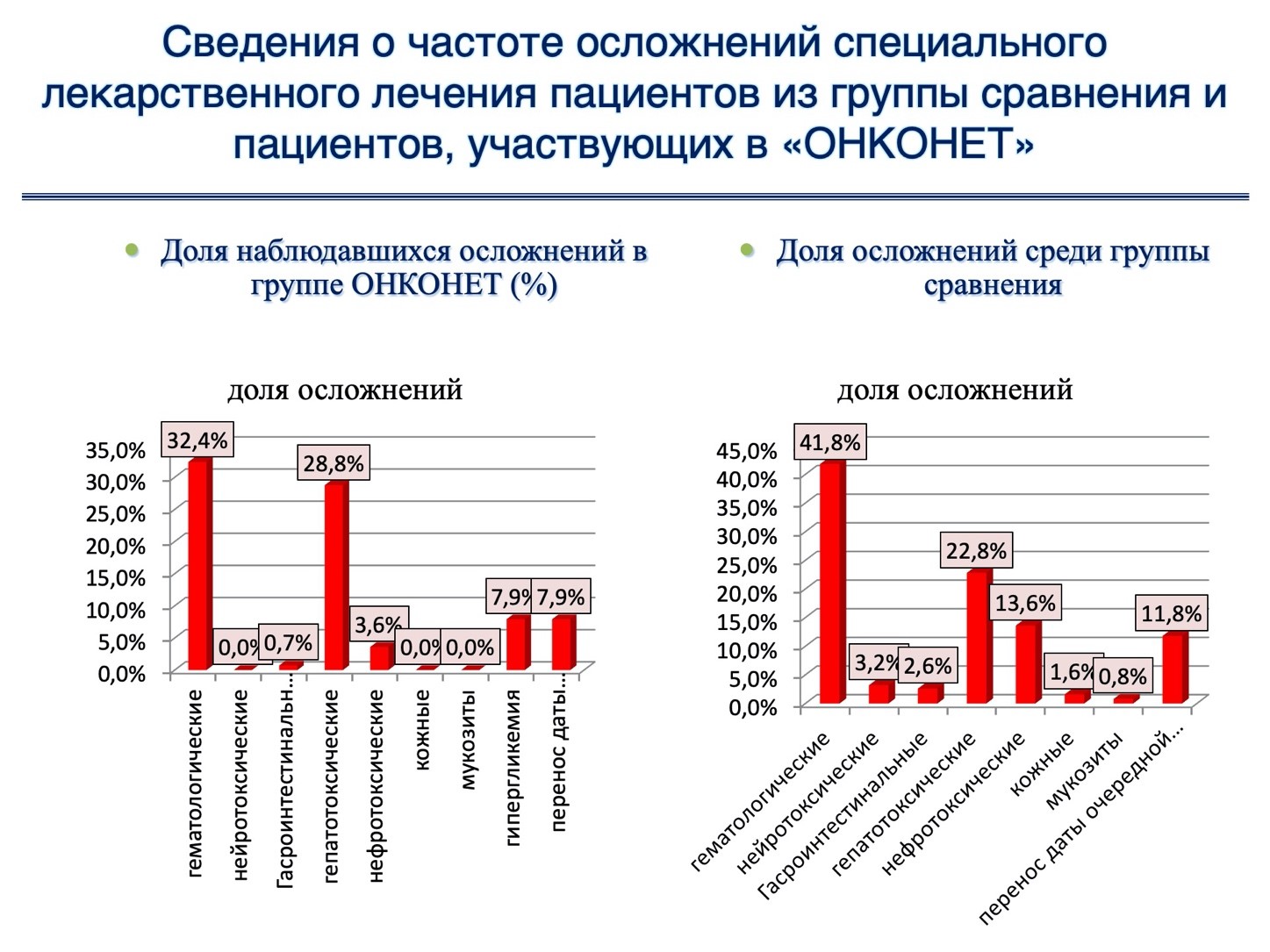
В исследуемой группе, в которой обеспечивался дистанционный врачебный мониторинг в системе ОНКОНЕТ, практически по всем параметрам выявились серьёзные преимущества. Своевременная коррекция лечения благодаря ОНКОНЕТ дала возможность уменьшить частоту осложнений, а некоторые из них свести к минимуму.
Среди наблюдавшихся осложнений в группе ОНКОНЕТ по сравнению с группой, проходящий обычное химиотерапевтическое лечение без мониторинга, реже наблюдались:
- на 10% – гематологические осложнения (32% в группе ОНКОНЕТ против 42% в контрольной);
- в 3 раза – нарушения работы в ЖКТ (0.7% против 2.6%);
- нейротоксические проявления практически сведены к минимуму (0% против 3.2%);
- в 4 раза – нефротоксичность (3.6% против 13.6%);
- сведены до минимума мукозиты и проявления кожной токсичности (0% – в группе ОНКОНЕТ против 08% и 1.6% – в контрольной); благодаря прикреплению пациентами к опросникам фотографий воспалений кожи эти явления обнаруживались на ранней стадии).
Главное, что с учетом этих результатов в полтора раза реже переносились даты очередного курсы химиотерапии (7.9% переносов в группе ОНКОНЕТ против 11.9% – в контрольной). В итоге это дало возможность выдерживать нужные интервалы между курсами лечения, что достоверно отличалось от контрольной группы, что в значительной степени улучшало выживаемость пациентов.
Обсуждение
Перенос многих привычных повседневных действий в дистанционную форму является мощнейшим трендом в финансовой сфере, торговле, коммуникациях и медиа и практически во всех сферах жизни. Однако, в медицине этот процесс идет значительно медленнее, в силу естественного консерватизма медицины, имеющей дело с самым дорогим – человеческой жизнью, а также в силу ряда организационных причин.
Создание и внедрение системы ОНКОНЕТ проходило по настоятельным просьбам пациентов Ассоциации онкологических пациентов «Здравствуй», транслировавших нам огромную заинтересованность онкологических пациентов в том, чтобы иметь постоянный канал мониторинга и взаимодействия с лечащим врачом даже за пределами медицинской организации. Глубокая заинтересованность хронических пациентов в такой медицинской услуге подтверждается опросом, проведенным нами в преддверии ежегодного Всероссийского конгресса пациентов.
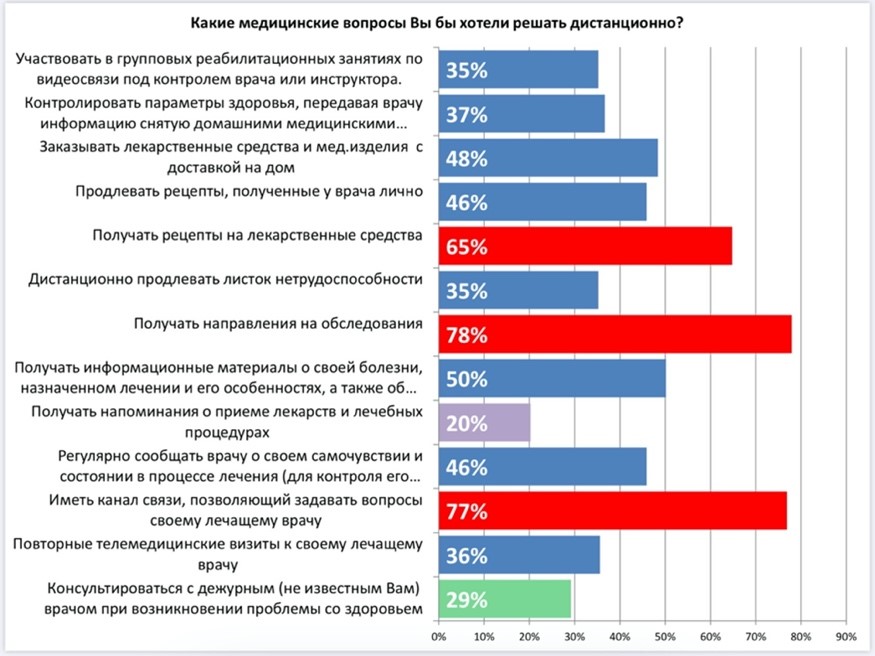
На Диаграмме 2 приведены результаты оценки востребованности различных дистанционных сервисов. 77% пациентов верят, что именно постоянный канал связи с врачом поможет снизить страх и не чувствовать себя «один на один» с последствиями токсического лечения и позволит не прерывать курс лечения из-за неконтролируемых осложнений. Востребованность этой услуги подтверждается также и тем фактом, что 36% опрошенных заинтересованных в ней пациентов готовы приобретать ее даже как дополнительную платную услугу.
Настоящее исследование является первым опытом доказательства эффективности дистанционного мониторинга в онкологии в России. Поскольку данное исследование не было спланировано заранее (в силу поэтапного инициативного внедрения системы по запросу пациентской организации). Исследование выполнено как ретроспективное. В дальнейшем бы хотелось провести более доказательное проспективное рандомизированное исследование, в ходе которого с помощью дополнительного анкетирования оценить влияние дистанционного мониторинга на качество жизни пациентов. Такая работа нами уже начата.
Однако, на фоне поиска научных доказательств эффективности, сама жизнь внесла неопровержимые доказательства важности дистанционного мониторинга онкологических пациентов. Уже в процессе подготовки настоящей статьи разразилась пандемия COVID-19, в самом начале которой Минздравом РФ было опубликовано специальное предупреждение о необходимости максимального сокращения контактов для онкологических пациентов [24]. И предлагаемая в данной статье система ОНКОНЕТ позволит стать одним из эффективных инструментов в решении этой проблемы.
Именно использование дистанционного мониторинга на дому позволит онкологическим пациентам строго соблюдать режим самоизоляции и сократить посещения медицинских организаций, оставаясь при этом под наблюдением своего лечащего врача.
В период пандемии в систему ОНКОНЕТ был интегрирован модуль, который по обученному алгоритму автоматизирует процесс выявления случаев COVID-19 среди онкобольных, проходящих лечение и наблюдение. В систему был добавлен специальный опросник, контролирующий у пациентов дополнительные параметры: гипер/гипотермии, брадипноэ, тахипноэ, гипоксемии, дисгевзии и др. Встроенный алгоритм автоматически выявлял и генерировал экстренные уведомления лечащему врачу, обращая его внимание на возможное развитие у пациента симптомов COVID-19.
Целью этого было сокращение количества визитов заболевшего пациента в онкодиспансер и снижение риска заражения и инфекционной нагрузки для других пациентов и врачей.
Очевидно, что протестированная в Липецке система дистанционного мониторинга пациентов на дому ОНКОНЕТ
Система ОНКОНЕТ сможет стать помощником для пациентов на иммунотерапии – поможет вести непрерывное долгосрочное дистанционное наблюдение за пациентами даже после прекращения терапии и может также стать эффективным инструментом мониторинга пациентов на иммунотерапии ингибиторами контрольных точек, такими как антитела к PD- (L) 1 и CTLA-4 [26-35]. Ингибиторы иммунной контрольной точки действуют посредством ингибирования блокирования Т-клеток, что приводит к гибели раковых клеток, опосредованной Т-клетками. Побочные эффекты ингибиторов иммунного контроля напоминают аутоиммунное заболевание. Наиболее распространенными являются сыпь, эндокринная токсичность, токсичность желудочно-кишечного тракта, гепатит и пневмонит. Могут возникнуть даже опасные для жизни побочные эффекты, которыми можно управлять с помощью раннего выявления, задержки или прекращения иммуноонкологической терапии и начала приема иммунодепрессантов, кортикостероидов [36-39]. Время возникновения побочных эффектов отличается от традиционной терапии рака, и они могут проявляться от нескольких месяцев до нескольких лет после начала терапии или после прекращения терапии [40-42], что делает длительное дистанционное наблюдение за пациентом чрезвычайно оправданным.
Документирование состояния и самочувствия пациентов может производиться с помощью «тепловой карты» ОНКОНЕТ, формируемой автоматически на основе ежедневно заполняемых пациентом опросников. Документирование лечения с помощью автоматической передачи «тепловой карты» в Региональную интегрированную медицинскую карту уже осуществлено нами в Санкт-Петербурге [25] при подключении городских онкологических ЛПУ Санкт-Петербургское ГБУЗ «Городской клинический онкологический диспансер», ГБУЗ «Санкт-Петербургский клинический научно-практический центр специализированных видов медицинской помощи» (онкологический).
Но самое главное – система ОНКОНЕТ позволит устранить необходимость ежедневного визита в дневной стационар частого визита или нахождения в круглосуточном стационаре только ради ежедневного получения таблетированного лекарственного препарата!
Выводы
Проведенное исследование демонстрирует безусловную полезность, а также высокую медицинскую эффективность дистанционного мониторинга онкологических пациентов, особенно на фоне пандемии и необходимой самоизоляции онкологических пациентов.
Дистанционный мониторинг также повысит экономическую эффективность проводимого лечения и сократит загрузку онкологического коечного фонда.
При этом дистанционный мониторинг, ведение и консультирование лечащим врачом крайне востребованы онкологическими пациентами, значительно снижают тревожность и повышают качество их жизни, удовлетворенность проводимым лечением, лояльность и приверженность проводимому лечению, ведение правильного, рекомендованного врачом образа жизни, что также способствует росту эффективности.
Чрезвычайно важно обеспечить возможность бесплатного предоставления услуг дистанционного мониторинга онкологическим пациентам. Для этого необходимо включить оплату услуг дистанционного мониторинга и консультирования онкологических пациентов в тариф ОМС.
Литература
1. Reilly CM, Bruner DW, Mitchell SA, Minasian LM, Basch E, Dueck AC et al (2013) A literature synthesis of symptom prevalence and severity in persons receiving active cancer treatment. Support Care Cancer 21(6):1525–1550. https://doi.org/10.1007/s00520-012-1688-0
2. Henry DH, Viswanathan HN, Elkin EP, Traina S, Wade S, Cella D (2008) Symptoms and treatment burden associated with cancer treatment: results from a cross-sectional national survey in the U.S. Support Care Cancer 16(7):791–801. https://doi.org/10.1007/s00520-007-0380-2
3. Laugsand EA, Sprangers MA, Bjordal K, Skorpen F, Kaasa S, Klepstad P (2010) Health care providers underestimate symptom intensities of cancer patients: a multicenter european study. Health Qual Life Outcomes 8:104–7525. https://doi.org/10.1186/1477-7525-8-104
4. Basch E, Jia X, Heller G, Barz A, Sit L, Fruscione M et al (2009) Adverse symptom event reporting by patients vs clinicians: relationships with clinical outcomes. J Natl Cancer Inst 101(23):1624–1632. https://doi.org/10.1093/jnci/djp386
5. Gilbert JE, Howell D, King S, Sawka C, Hughes E, Angus H et al (2012) Quality improvement in cancer symptom assessment and control: the provincial palliative care integration project (PPCIP). J Pain Symptom Manag 43(4):663–678. https://doi.org/10.1016/j.jpainsymman.2011.04.028
6. Valderas JM, Kotzeva A, Espallargues M, Guyatt G, Ferrans CE, Halyard MY et al (2008) The impact of measuring patient-reported outcomes in clinical practice: a systematic review of the literature. Qual Life Res 17(2):179–193. https://doi.org/10.1007/s11136-007-9295-0
7. Velikova G, Booth L, Smith AB, Brown PM, Lynch P, Brown JM et al (2004) Measuring quality of life in routine oncology practice improves communication and patient well-being: a randomized controlled trial. J Clin Oncol 22(4):714–724. https://doi.org/10.1200/JCO.2004.06.078
8. Trajkovic-Vidakovic M, de Graeff A, Voest EE, Teunissen SC (2012) Symptoms tell it all: a systematic review of the value of symptom assessment to predict survival in advanced cancer patients. Crit Rev Oncol Hematol 84(1):130–148. https://doi.org/10.1016/j.critrevonc.2012.02.011
9. Benze G, Nauck F, Alt-Epping B, Gianni G, Bauknecht T, Ettl J, Munte A, Kretzschmar L, Gaertner J (2017) PROutine: a feasibility study assessing surveillance of electronic patient reported outcomes and adherence via smartphone app in advanced cancer. Ann Palliat Med. https://doi.org/10.21037/apm.2017.07.05
10. Jensen RE, Snyder CF, Abernethy AP, Basch E, Potosky AL, Roberts AC et al (2014) Review of electronic patient-reported outcomes systems used in cancer clinical care. J Oncol Pract 10(4):e215–e222. https://doi.org/10.1200/JOP.2013.001067
11. Kotronoulas G, Kearney N, Maguire R, Harrow A, Di Domenico D, Croy S et al (2014) What is the value of the routine use of patient-reported outcome measures toward improvement of patient outcomes, processes of care, and health service outcomes in cancer care? A systematic review of controlled trials. J Clin Oncol 32(14):1480–1501. https://doi.org/10.1200/JCO.2013.53.5948
12. Bennett AV, Jensen RE, Basch E (2012) Electronic patient-reported outcome systems in oncology clinical practice. CA Cancer J Clin 62(5):337–347. https://doi.org/10.3322/caac.21150
13. Cleeland CS, Wang XS, Shi Q, Mendoza TR, Wright SL, Berry MD et al (2011) Automated symptom alerts reduce postoperative symptom severity after cancer surgery: a randomized controlled clinical trial. J Clin Oncol 29(8):994–1000. https://doi.org/10.1200/JCO.2010.29.8315
14. Holch P, Warrington L, Bamforth LCA, Keding A, Ziegler LE, Absolom K et al (2017) Development of an integrated electronic platform for patient self-report and management of adverse events during cancer treatment. Ann Oncol 28(9):2305–2311. https://doi.org/10.1093/annonc/mdx317
15. Mullen KH, Berry DL, Zierler BK (2004) Computerized symptom and quality-of-life assessment for patients with cancer part II: acceptability and usability. Oncol Nurs Forum 31(5):E84–E89. https://doi.org/10.1188/04.ONF.E84-E89
16. Pakhomov SV, Jacobsen SJ, Chute CG, Roger VL (2008) Agreement between patient-reported symptoms and their documentation in the medical record. Am J Manag Care 14(8):530–539
17. Basch E, Deal AM, Kris MG, Scher HI, Hudis CA, Sabbatini P et al (2016) Symptom monitoring with patient-reported outcomes during routine cancer treatment: a randomized controlled trial. J Clin Oncol 34(6):557–565. https://doi.org/10.1200/JCO.2015.63.0830
18. Denis F, Yossi S, Septans AL, Charron A, Voog E, Dupuis O et al (2017a) Improving survival in patients treated for a lung cancer using self-evaluated symptoms reported through a web application. Am J Clin Oncol 40(5):464–469. https://doi.org/10.1097/COC.0000000000000189
19. Denis F, Lethrosne C, Pourel N, Molinier O, Pointreau Y, Domont J et al (2017b) Randomized trial comparing a web-mediated follow-up with routine surveillance in lung cancer patients. J Natl Cancer Inst 109(9): https://doi.org/10.1093/jnci/djx029
20. Basch E, Deal AM, Dueck AC, Scher HI, Kris MG, Hudis C et al (2017) Overall survival results of a trial assessing patient-reported outcomes for symptom monitoring during routine cancer treatment. JAMA 318(2):197–198. https://doi.org/10.1001/jama.2017.7156
25. https://www.cnews.ru/news/line/2020-05-15_netrika_provela_pilotnoe
26. Brahmer JR, Rodriguez-Abreu D, Robinson AG, Hui R, Csoszi T, Fulop A et al (2017) Health-related quality-of-life results for pembrolizumab versus chemotherapy in advanced, PD-L1-positive NSCLC (KEYNOTE-024): a multicentre, international, randomised, open-label phase 3 trial. Lancet Oncol 18(12):1600–1609
27. Wolchok JD, Chiarion-Sileni V, Gonzalez R, Rutkowski P, Grob JJ, Cowey CL et al (2017) Overall survival with combined nivolumab and ipilimumab in advanced melanoma. N Engl J Med 377(14):1345–1356. https://doi.org/10.1056/NEJMoa1709684
28. Borghaei H, Paz-Ares L, Horn L, Spigel DR, Steins M, Ready NE et al (2015) Nivolumab versus docetaxel in advanced nonsquamous non-small-cell lung cancer. N Engl J Med 373(17):1627–1639. https://doi.org/10.1056/NEJMoa1507643
29. Motzer RJ, Escudier B, McDermott DF, George S, Hammers HJ, Srinivas S et al (2015) Nivolumab versus everolimus in advanced renal-cell carcinoma. N Engl J Med 373(19):1803–1813. https://doi.org/10.1056/NEJMoa1510665
30. Bellmunt J, de Wit R, Vaughn DJ, Fradet Y, Lee JL, Fong L et al (2017) Pembrolizumab as second-line therapy for advanced urothelial carcinoma. N Engl J Med 376(11):1015–1026. https://doi.org/10.1056/NEJMoa1613683
31. Robert C, Schachter J, Long GV, Arance A, Grob JJ, Mortier L et al (2015a) Pembrolizumab versus ipilimumab in advanced melanoma. N Engl J Med 372(26):2521–2532. https://doi.org/10.1056/NEJMoa1503093
32. Robert C, Long GV, Brady B, Dutriaux C, Maio M, Mortier L et al (2015b) Nivolumab in previously untreated melanoma without BRAF mutation. N Engl J Med 372(4):320–330. https://doi.org/10.1056/NEJMoa1412082
33. Herbst RS, Baas P, Kim DW, Felip E, Perez-Gracia JL, Han JY et al (2016) Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): a randomised controlled trial. Lancet 387(10027):1540–1550. https://doi.org/10.1016/S0140-6736(15)01281-7
34. Rittmeyer A, Barlesi F, Waterkamp D, Park K, Ciardiello F, von Pawel J et al (2017) Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer (OAK): a phase 3, open-label, multicentre randomised controlled trial. Lancet 389(10066):255–265
35. Reck M, Rodriguez-Abreu D, Robinson AG, Hui R, Csoszi T, Fulop A et al (2016) Pembrolizumab versus chemotherapy for PD-L1-positive non-small-cell lung cancer. N Engl J Med 375(19):1823–1833. https://doi.org/10.1056/NEJMoa1606774
36. Spain L, Diem S, Larkin J (2016) Management of toxicities of immune checkpoint inhibitors. Cancer Treat Rev 44:51–60. https://doi.org/10.1016/j.ctrv.2016.02.001
37. Puzanov I, Diab A, Abdallah K, Bingham CO 3rd, Brogdon C, Dadu R et al (2017) Managing toxicities associated with immune checkpoint inhibitors: consensus recommendations from the society for immunotherapy of cancer (SITC) toxicity management working group. J Immunother Cancer 5(1):95-017. https://doi.org/10.1186/s40425-017-0300-z
38. Haanen JBAG, Carbonnel F, Robert C, Kerr KM, Peters S, Larkin J et al (2018) Management of toxicities from immunotherapy: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. https://doi.org/10.1093/annonc/mdy162
39. Wang DY, Salem JE, Cohen JV, Chandra S, Menzer C, Ye F et al (2018) Fatal toxic effects associated with immune checkpoint inhibitors: a systematic review and meta-analysis. JAMA Oncol. https://doi.org/10.1001/jamaoncol.2018.3923
40. Li H, Ma W, Yoneda KY, Moore EH, Zhang Y, Pu LL et al (2017) Severe nivolumab-induced pneumonitis preceding durable clinical remission in a patient with refractory, metastatic lung squamous cell cancer: a case report. J Hematol Oncol 10(1):64-017. https://doi.org/10.1186/s13045-017-0433-z
41. McDermott DF, Drake CG, Sznol M, Choueiri TK, Powderly JD, Smith DC et al (2015) Survival, durable response, and long-term safety in patients with previously treated advanced renal cell carcinoma receiving nivolumab. J Clin Oncol 33(18):2013–2020. https://doi.org/10.1200/JCO.2014.58.1041
42. Weber JS, Hodi FS, Wolchok JD, Topalian SL, Schadendorf D, Larkin J et al (2017) Safety profile of nivolumab monotherapy: a pooled analysis of patients with advanced melanoma. J Clin Oncol 35(7):785–792. https://doi.org/10.1200/JCO.2015.66.1389
-
Рак и его типы
-
Лечение
- Химиотерапия
- Лучевая терапия
- Хирургическое лечение
- Клинические исследования
- Гормонотерапия (эндокринотерапия)
- Поддерживающая терапия
- Осложнения лечения и их коррекция
- Лечебное питание
- ВАХД-инновационный метод лечения
- РНЦХ имени акад. Б.В. Петровского
- Радионуклидная альфа-терапия
- Профилактика нежелательных явлений
-
Это надо знать
-
Помощь
- Профилактика





